¿Qué son los cofactores? - Las moléculas que activan las enzimas.
Las enzimas son los minúsculos caballos de trabajo de los sistemas biológicos, catalizando innumerables reacciones químicas necesarias para la vida. Son proteínas especializadas que aceleran (o ralentizan) las reacciones químicas al reducir la energía de activación necesaria para iniciarlas. Como las llaves en una cerradura, las enzimas encajan perfectamente con moléculas específicas, llamadas sustratos, para realizar su función.
Sin embargo, las enzimas no pueden funcionar solas; a menudo requieren la ayuda de pequeñas moléculas llamadas cofactores. Los cofactores actúan como activadores o inhibidores de la actividad enzimática y son esenciales para una función enzimática adecuada. Estas diminutas moléculas pueden considerarse como "bujías" que encienden las reacciones enzimáticas y las mantienen funcionando eficientemente.
En este artículo, exploraremos qué son los cofactores, cómo funcionan y por qué son tan importantes en los sistemas biológicos.
Introducción a las enzimas y su función.
Las enzimas son catalizadores biológicos esenciales que aceleran las reacciones químicas en los organismos vivos. Juegan un papel crucial en el metabolismo y están involucradas en casi todos los procesos bioquímicos que ocurren dentro de las células. La cinética enzimática se refiere al estudio de estas moléculas y su actividad, incluyendo cómo funcionan, interactúan con los sustratos y son reguladas.
Un aspecto clave de la función enzimática es la especificidad del sustrato. Cada enzima tiene una molécula objetivo específica o conjunto de moléculas que puede catalizar. Esta especificidad surge de la forma tridimensional única del sitio activo de la enzima, que encaja perfectamente con su(s) sustrato(s) objetivo. La interacción entre la enzima y el sustrato es altamente específica y a menudo implica múltiples interacciones débiles que permiten un control preciso sobre las velocidades de reacción.
La función enzimática también está sujeta a la regulación por diversos factores, incluyendo cofactores. Estas moléculas ayudan en el proceso catalítico al unirse a las enzimas y alterar su actividad. En la siguiente sección, exploraremos en más detalle la definición y los tipos de cofactores.
Definición y Tipos de Cofactores
Los cofactores son moléculas esenciales que se unen a las enzimas, activándolas o estabilizándolas. Estos cofactores se pueden dividir en dos categorías principales: orgánicos e inorgánicos. Las coenzimas son cofactores orgánicos que ayudan a las enzimas a realizar su función, mientras que los grupos prostéticos son componentes no proteicos que se convierten en una parte permanente de la estructura de la enzima. Comprender los diferentes tipos de cofactores es crucial para comprender cómo funcionan las enzimas y cómo se pueden manipular para varias aplicaciones.
Cofactores orgánicos e inorgánicos
La activación de enzimas es facilitada por cofactores orgánicos e inorgánicos, los cuales son esenciales para el correcto funcionamiento de las vías metabólicas. Los cofactores orgánicos, como las coenzimas, son moléculas complejas que se unen débilmente al sitio activo de la enzima. Normalmente son derivados de vitaminas o aminoácidos y juegan un papel crucial en la transferencia de grupos químicos entre enzimas durante las reacciones metabólicas.
Por otro lado, los cofactores inorgánicos suelen ser iones metálicos que ayudan a estabilizar la estructura de la enzima y facilitan las reacciones de transferencia de electrones. Pueden encontrarse en diversas fuentes como minerales, agua o aire. Los cofactores inorgánicos juegan un papel importante en las reacciones enzimáticas que involucran química redox donde los electrones son transferidos de una molécula a otra.
A medida que avanzamos en nuestra discusión sobre coenzimas y grupos prostéticos, es importante destacar que estas moléculas también actúan como cofactores orgánicos que apoyan la actividad enzimática.
Coenzimas y Grupos Prostéticos
Como las piezas intrincadas de un rompecabezas, las coenzimas y los grupos prostéticos encajan perfectamente en los sitios activos de sus respectivas enzimas, brindando un soporte crítico para la actividad enzimática. Las coenzimas son moléculas orgánicas que trabajan con las enzimas para realizar reacciones catalíticas en las vías metabólicas. A menudo participan en reacciones de oxidación-reducción mediante la transferencia de electrones o grupos funcionales entre moléculas. Ejemplos de coenzimas incluyen NAD +, FAD y coenzima A.
Por otro lado, los grupos prostéticos son componentes no proteicos que están permanentemente unidos a una enzima y ayudan en su función. Estos grupos pueden ser orgánicos o inorgánicos y pueden cumplir una variedad de funciones como la transferencia de electrones o la unión de sustratos. Algunos ejemplos de grupos prostéticos incluyen el hemo en la hemoglobina y los citocromos, así como el flavin mononucleótido (FMN) unido a la glucosa oxidasa.
Como hemos visto, las coenzimas y los grupos prostéticos son jugadores esenciales en las reacciones enzimáticas dentro de las vías metabólicas. En la próxima sección, exploraremos cómo estos cofactores activan las enzimas para llevar a cabo sus funciones específicas.
Cómo los cofactores activan las enzimas
Los cambios estructurales en las enzimas desempeñan un papel crucial en facilitar las reacciones químicas, y a menudo son desencadenados por la unión de cofactores al sitio activo de la enzima. Este proceso conduce a cambios conformacionales que permiten que la enzima interactúe mejor con su sustrato, disminuyendo la energía de activación requerida para que ocurra la reacción. Comprender cómo los cofactores activan las enzimas es esencial para elucidar los mecanismos subyacentes a muchos procesos biológicos.
Cambios estructurales en enzimas.
Comprender las formas en que las enzimas experimentan cambios estructurales es esencial para comprender su actividad catalítica y función general. Las enzimas son biomoléculas complejas que requieren cambios conformacionales específicos para realizar su función de facilitar reacciones químicas.
Estos cambios conformacionales a menudo son inducidos por cofactores, que pueden alterar la forma de la enzima y crear un entorno más favorable para la unión del sustrato. Los cambios estructurales que ocurren en las enzimas pueden explicarse a través de la cinética enzimática, que se refiere al estudio de cómo las enzimas interactúan con los sustratos y productos durante una reacción.
Para apreciar completamente los cambios estructurales que ocurren en las enzimas, es importante considerar varios factores clave. En primer lugar, las enzimas tienen sitios activos que se unen a sustratos específicos y facilitan la reacción química.
En segundo lugar, los cofactores pueden unirse a otras regiones en la molécula de la enzima, causando cambios conformacionales que afectan la forma y reactividad del sitio activo hacia su sustrato. Finalmente, la cinética enzimática gobierna la rapidez con que ocurren estas reacciones midiendo parámetros como la concentración del sustrato y la velocidad de reacción.
Facilitar reacciones químicas implica no solo comprender la dinámica estructural de las enzimas, sino también evaluar cómo trabajan en conjunto con otras biomoléculas para generar energía o llevar a cabo procesos metabólicos.

Facilitando Reacciones Químicas
Facilitar las reacciones químicas requiere una comprensión integral de la interacción entre enzimas y otras biomoléculas, así como una apreciación por la intrincada danza de interacciones moleculares que permiten que los procesos vitales se lleven a cabo.
Las enzimas son proteínas que catalizan reacciones químicas específicas al reducir la energía de activación necesaria para que estas reacciones ocurran. Sin embargo, las enzimas no pueden funcionar solas; requieren la ayuda de cofactores, que son moléculas no proteicas que activan o regulan la actividad enzimática.
Los cofactores desempeñan un papel crítico en el metabolismo al facilitar las principales reacciones químicas. Algunos cofactores actúan como transportadores de electrones, permitiendo que las enzimas transfieran electrones entre moléculas durante las reacciones de oxidación-reducción. Otros cofactores ayudan a estabilizar los complejos enzima-sustrato o ayudan en la unión del sustrato.
Además de sus roles en las vías metabólicas, los cofactores también están involucrados en la regulación enzimática. Por ejemplo, ciertos cofactores pueden actuar como moduladores alostéricos y unirse a sitios reguladores en las enzimas para activar o inhibir su actividad. Comprender el papel de los cofactores es esencial para comprender cómo funcionan los sistemas biológicos a nivel molecular y cómo podemos manipularlos con fines terapéuticos.
Como se mencionó anteriormente, la actividad enzimática a menudo requiere la ayuda de sus socios no proteicos - cofactores. En la siguiente sección, exploraremos ejemplos de enzimas y sus cofactores correspondientes y profundizaremos en la compleja interacción entre estas biomoléculas en los procesos bioquímicos.
Ejemplos de enzimas y sus cofactores.
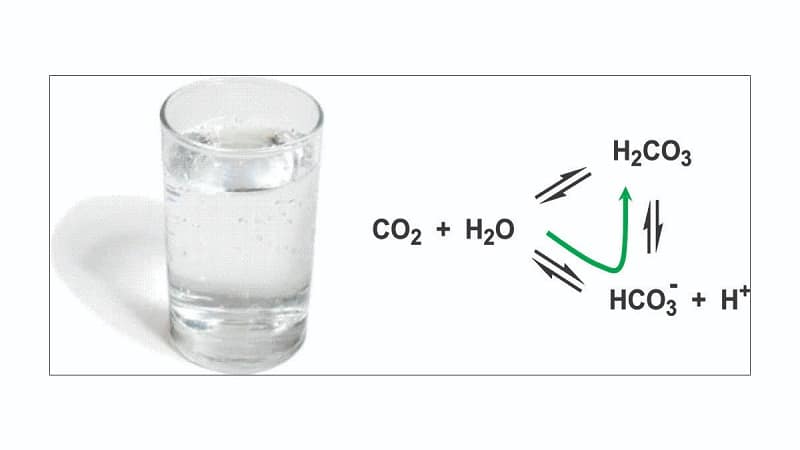
La identificación de enzimas específicas y sus cofactores correspondientes es crucial para comprender los procesos bioquímicos subyacentes que regulan la actividad enzimática. La especificidad de la enzima se refiere al hecho de que cada enzima solo puede catalizar una reacción particular, lo que significa que la presencia o ausencia de un cofactor específico puede afectar en gran medida su actividad. Por ejemplo, sin iones de zinc como cofactor requerido, la anhidrasa carbónica no podría catalizar la hidratación del CO2 a HCO3-, lo que es esencial para regular el pH en la sangre y otros fluidos corporales.
Otro aspecto importante a considerar al hablar de enzimas y sus cofactores es la importancia de la concentración del cofactor. En general, las bajas concentraciones de un cofactor requerido pueden llevar a una disminución de la actividad enzimática debido a la disponibilidad limitada para la unión con la enzima.
Por el contrario, las altas concentraciones de ciertos cofactores pueden resultar en interacciones no específicas con otras moléculas, lo que lleva a efectos potencialmente perjudiciales dentro de los sistemas biológicos. Por lo tanto, mantener niveles apropiados de cofactores es fundamental para una función enzimática óptima.
En general, comprender ejemplos de enzimas y sus cofactores correspondientes proporciona información sobre cómo estas moléculas trabajan juntas para facilitar reacciones químicas dentro de los sistemas biológicos. La próxima sección profundizará en la importancia de estos coenzimas en el mantenimiento de la homeostasis dentro de los organismos vivos.
Importancia de los cofactores en los sistemas biológicos
Ejemplos de enzimas y sus cofactores han sido discutidos previamente, ¿pero cuál es la importancia de los cofactores en los sistemas biológicos? Los cofactores juegan un papel crucial en las vías metabólicas al activar enzimas y regular su actividad. Sin ellos, muchos procesos importantes en el cuerpo no ocurrirían o ocurrirían a una tasa insuficiente.
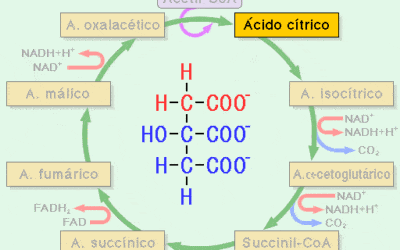
Un ejemplo de la importancia de un cofactor se ve en el proceso de la respiración celular. La enzima piruvato deshidrogenasa requiere tiamina pirofosfato como cofactor para convertir el piruvato en acetil-CoA, que luego puede ingresar al ciclo del ácido cítrico. Sin que esta reacción ocurra de manera eficiente, la producción de ATP se reduciría significativamente y el metabolismo energético se vería afectado.
Los cofactores también juegan un papel en la regulación de la actividad enzimática. Un ejemplo se ve con la regulación alostérica, donde una molécula se une a una enzima en un sitio que no es su sitio activo y cambia su forma, alterando así su actividad. De esta manera, los cofactores pueden actuar como interruptores moleculares para procesos enzimáticos que necesitan ser encendidos o apagados según las necesidades de la célula.
Si bien las enzimas son necesarias para que ocurran muchos procesos biológicos, a menudo requieren cofactores para funcionar correctamente. Estas moléculas activan enzimas y regulan su actividad a través de varios mecanismos, como la regulación alostérica. Comprender estos mecanismos proporciona información sobre cómo se regulan las vías metabólicas dentro de las células y destaca la importancia de estudiar tanto las enzimas como sus cofactores asociados.
Preguntas frecuentes
¿Cómo se sintetizan los cofactores en el cuerpo?
Los cofactores son moléculas esenciales que activan enzimas, permitiéndoles realizar sus funciones catalíticas. Estas pequeñas moléculas orgánicas o inorgánicas juegan un papel crucial en la regulación de la actividad enzimática y el mantenimiento de las vías metabólicas.
Mientras que algunos cofactores son producidos en el cuerpo, otros deben ser obtenidos de fuentes externas como la dieta o los suplementos. El proceso de síntesis de cofactores endógenos implica complejas vías bioquímicas que requieren enzimas y sustratos específicos.
Por ejemplo, la coenzima Q10 se sintetiza a partir de tirosina a través de una serie de reacciones enzimáticas que involucran múltiples compuestos intermedios. De manera similar, la hemo se sintetiza a través de una vía multietapas que involucra varias enzimas y cofactores como el hierro y la vitamina B6.
En general, la biosíntesis de cofactores está estrechamente regulada para garantizar una función enzimática óptima y una homeostasis metabólica en el cuerpo.
¿Pueden las enzimas funcionar sin cofactores?
La importancia de los cofactores en la cinética enzimática no puede ser subestimada. Los cofactores son moléculas no proteicas que se unen a las enzimas y activan o modulan su actividad. Se pueden clasificar en dos tipos: iones metálicos y moléculas orgánicas, también conocidas como coenzimas.
Si bien hay algunos ejemplos de enzimas que no requieren cofactores, la mayoría de las enzimas dependen de estas moléculas para funcionar de manera óptima. Por ejemplo, sin cofactores como iones de magnesio o zinc, las nucleasas no podrían cortar el ADN eficientemente. De manera similar, sin hemo como cofactor, las enzimas del citocromo P450 no podrían desempeñar su papel esencial en el metabolismo de los fármacos.
En general, la presencia o ausencia de cofactores juega un papel crítico en la determinación de la actividad catalítica y la especificidad de muchas enzimas.
¿Cuál es la diferencia entre un cofactor y una coenzima?
Mientras que las enzimas catalizan reacciones bioquímicas, a menudo requieren la ayuda de cofactores para funcionar correctamente. Los cofactores pueden ser moléculas inorgánicas u orgánicas que trabajan junto con las enzimas para aumentar su actividad y especificidad.
En contraste, las coenzimas son compuestos orgánicos que se unen al sitio activo de una enzima y actúan como portadores de grupos químicos o electrones durante las reacciones. Ejemplos de cofactores en enzimas incluyen iones metálicos como hierro, zinc y magnesio, así como moléculas orgánicas como el dinucleótido de adenina flavín (FAD) y el dinucleótido de adenina nicotinamida (NAD +).
Sin estos cofactores esenciales, muchas reacciones enzimáticas no pueden ocurrir eficientemente, lo que destaca el papel crucial que desempeñan en el metabolismo celular.
¿Cómo afectan los cofactores a la especificidad de las enzimas?
Los mecanismos de activación de cofactores juegan un papel vital en la especificidad de las enzimas. Las enzimas requieren sustratos específicos para catalizar reacciones, y la presencia de cofactores puede aumentar la afinidad entre las enzimas y sus sustratos. Esto se logra a través de varios mecanismos como la regulación alostérica, la unión de iones metálicos y la modificación covalente.
Los cofactores también pueden alterar las propiedades catalíticas de la enzima al estabilizar los intermediarios de reacción o facilitar la transferencia de electrones. Además, la cinética de la unión del sustrato de la enzima se ve afectada por los cofactores, ya que pueden alterar la tasa de asociación y disociación entre el complejo enzima-sustrato.
Por lo tanto, comprender cómo los cofactores afectan la especificidad de las enzimas proporciona información sobre procesos biológicos fundamentales y puede ayudar en el descubrimiento de medicamentos y aplicaciones industriales.
¿Se puede usar el mismo cofactor por diferentes enzimas?
Los cofactores son moléculas esenciales que activan las enzimas y mejoran su actividad catalítica. Estas moléculas pueden ser orgánicas o inorgánicas y desempeñan un papel crucial en la especificidad de las enzimas.
Es interesante observar que algunas enzimas comparten los mismos cofactores, lo que demuestra la versatilidad de estas moléculas en reacciones enzimáticas. Por ejemplo, tanto la piruvato deshidrogenasa como la alfa-cetoglutarato deshidrogenasa utilizan el pirofosfato de tiamina como cofactor.
Además, la concentración de cofactores es fundamental para lograr una actividad enzimática óptima. La falta de suficientes concentraciones de cofactores puede reducir la velocidad de las reacciones enzimáticas. Por otro lado, un exceso de cofactores puede tener efectos tóxicos en las células.
Por lo tanto, comprender la importancia de los cofactores compartidos entre las enzimas y monitorear sus concentraciones es vital para el correcto funcionamiento de las enzimas y la salud celular en general.
Conclusión
Los cofactores son moléculas esenciales que activan enzimas en sistemas biológicos. Vienen en dos tipos, a saber, cofactores orgánicos e inorgánicos, y desempeñan un papel vital en garantizar que las reacciones enzimáticas ocurran de manera eficiente. A través de varios mecanismos como reacciones redox y formación de complejos enzima-sustrato, los cofactores aumentan la actividad catalítica de las enzimas al estabilizar sus estructuras o participar directamente en la reacción.
La importancia de los cofactores no puede ser exagerada ya que están involucrados en numerosos procesos metabólicos necesarios para la vida. Sin ellos, muchas enzimas no funcionarían correctamente, lo que llevaría a diversas enfermedades y trastornos. La relación entre las enzimas y sus cofactores a menudo se asemeja a la de una cerradura y una llave: la enzima es la cerradura mientras que el cofactor es la llave que la desbloquea.
En esencia, trabajan juntos sin problemas para garantizar que las reacciones bioquímicas eficientes se lleven a cabo dentro de los organismos vivos. Como dijo una vez Ralph Waldo Emerson: 'La naturaleza nunca se apresura; átomo por átomo, poco a poco logra su trabajo'.
Al igual que el lento pero constante progreso de la naturaleza hacia la perfección, las reacciones enzimáticas dependen de la activación proporcionada por los cofactores para lograr la eficiencia óptima. Por lo tanto, podemos apreciar lo importantes que son estas pequeñas pero poderosas moléculas para mantener la vida en la Tierra a través de las vías bioquímicas que subyacen a todos los procesos fisiológicos, desde la respiración celular hasta la replicación del ADN.
Si quieres conocer otros artículos parecidos a ¿Qué son los cofactores? - Las moléculas que activan las enzimas. puedes visitar la categoría Bioquímica.
Deja una respuesta



¡Más Contenido!