¿Por qué las proteínas prion son peligrosas? - La amenaza silenciosa.
Las proteínas priónicas son un grupo enigmático de proteínas que se sabe que causan una variedad de enfermedades neurodegenerativas fatales en humanos y animales. A pesar de los avances significativos en el campo de la investigación de los priones, los mecanismos moleculares detrás de su patogenicidad siguen siendo poco comprendidos.
El objetivo de este artículo es explorar los peligros que presentan las proteínas priónicas y por qué se consideran una amenaza silenciosa.
Los priones son únicos en que carecen de ácidos nucleicos y pueden autoreplicarse a través del plegamiento incorrecto, lo que resulta en la formación de agregados enriquecidos con láminas β conocidos como fibrillas amiloides. Estas fibrillas se acumulan dentro de las neuronas, lo que conduce a la disfunción celular y, en última instancia, a la muerte neuronal.
Debido a su capacidad de autoreplicación, incluso pequeñas cantidades de priones infecciosos pueden provocar la transmisión de enfermedades. Además, los priones han demostrado ser resistentes a los métodos de esterilización tradicionales como el tratamiento térmico o la desinfección química, lo que los hace particularmente difíciles de controlar.
A medida que profundizamos en los mecanismos detrás de la patogénesis de los priones, se hace cada vez más evidente por qué estas proteínas representan una amenaza significativa tanto médica como ambientalmente.
- Comprendiendo las proteínas priónicas
- El peligro del plegamiento incorrecto.
- Resistencia a los métodos de esterilización tradicionales.
- Medidas de prevención y control
- Investigación actual y direcciones futuras
-
Preguntas frecuentes
- ¿Cuál es la historia de la investigación y el descubrimiento de los priones?
- ¿Las enfermedades por priones se pueden transmitir de animales a humanos?
- ¿Cómo afectan las proteínas priónicas al cerebro y al sistema nervioso?
- ¿Existen tratamientos conocidos para las enfermedades por priones?
- ¿Cómo se diferencian las enfermedades priónicas de otras enfermedades neurodegenerativas, como el Alzheimer o el Parkinson?
- Conclusión
Comprendiendo las proteínas priónicas
El estudio de las proteínas priónicas es crucial para comprender sus posibles riesgos y efectos en los sistemas biológicos. Las proteínas priónicas son inusuales porque pueden plegarse en diferentes formas, lo que lleva a la formación de fibras amiloides que se agregan y depositan en los tejidos. La estructura de las proteínas priónicas se caracteriza por una alta proporción de láminas beta, lo que las hace resistentes a la degradación por proteasas.
Las proteínas priónicas se han asociado con varias enfermedades neurodegenerativas, incluyendo la enfermedad de Creutzfeldt-Jakob (ECJ), la insomnio familiar fatal (IFF) y el síndrome de Gerstmann-Sträussler-Scheinker (GSS). Estas enfermedades son causadas por la acumulación de priones mal plegadas en el cerebro, lo que lleva a la disfunción neuronal y la muerte. Aún no se comprende completamente cómo ocurre este mal plegamiento, pero se ha sugerido que las mutaciones en el gen PRNP que codifica para la proteína priónica pueden desempeñar un papel.
Comprender los mecanismos detrás del plegamiento y mal plegamiento de las proteínas priónicas es crucial para identificar posibles objetivos terapéuticos para estas enfermedades devastadoras. Sin embargo, como veremos en la siguiente sección, los priones mal plegadas representan un peligro aún mayor debido a su capacidad para convertir los priones normales en agentes infecciosos a través de un proceso conocido como templado.
El peligro del plegamiento incorrecto.
Las proteínas priónicas son notorias por su capacidad de plegarse incorrectamente, lo que lleva a la formación de agregados y conglomerados que pueden tener efectos devastadores en las células y tejidos. Cuando las proteínas priónicas se pliegan incorrectamente, pueden adoptar una conformación rica en láminas beta que les permite agregarse con otras moléculas priónicas, formando una compleja red de interacciones intermoleculares.
Estos agregados y conglomerados pueden interrumpir los procesos celulares y contribuir al desarrollo de enfermedades neurodegenerativas como la enfermedad de Creutzfeldt-Jakob (ECJ) y la enfermedad de Alzheimer.
Cómo se produce el mal plegamiento de las proteínas priónicas.
A través de un proceso de malplegado, las proteínas prion adquieren una conformación anormal que conduce a la formación de agregados y el subsiguiente daño del tejido neural. La propagación de la proteína prion depende de su capacidad para inducir a otras proteínas normales a adoptar la misma configuración malplegada. Esto se logra a través de un mecanismo complejo que implica la interacción directa entre diferentes regiones de la proteína y factores celulares, como chaperonas y cofactores.
Los mecanismos de malplegado pueden ser desencadenados por mutaciones genéticas, modificaciones post-traduccionales o factores ambientales que afectan la estabilidad de la conformación nativa. Estos cambios conducen a alteraciones en las estructuras secundarias o terciarias, exponiendo superficies hidrofóbicas que promueven la agregación con otras moléculas.
Los cúmulos resultantes pueden variar desde pequeños oligómeros hasta grandes fibrillas que son resistentes a la degradación proteolítica. En última instancia, estos agregados se acumulan en áreas específicas del cerebro y causan pérdida neuronal y disfunción sináptica.
Esta acumulación desencadena una reacción en cascada que amplifica aún más los eventos de malplegado y genera especies más tóxicas. Por lo tanto, comprender cómo las proteínas prion se malpliegan es crucial para desarrollar estrategias para prevenir su propagación y mitigar sus efectos perjudiciales sobre la función neurológica.
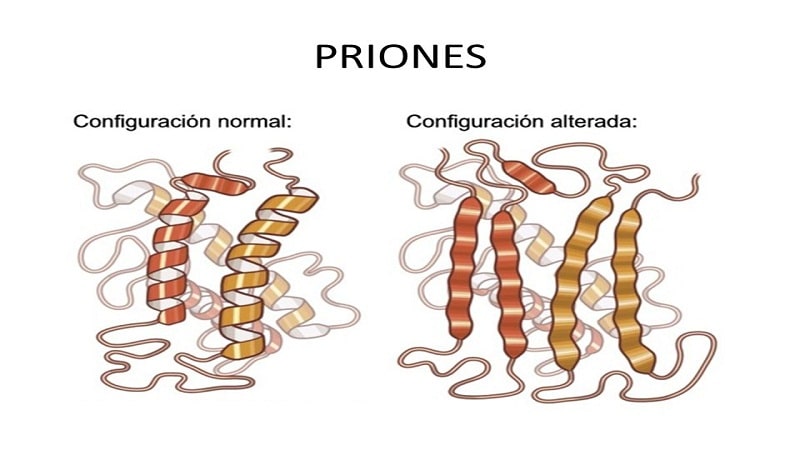
Formación de agregados y grumos
La formación de agregados y grupos es una hazaña notable de las proteínas priónicas, destacando su capacidad para inducir a otras proteínas normales a adoptar la misma configuración mal plegada y amplificar aún más los eventos de mal plegamiento. Los priones son notorios por sus mecanismos de agregación, que involucran la formación de fibrillas amiloides que se acumulan en los tejidos cerebrales y causan consecuencias patológicas.
La formación de estos agregados se inicia por la interacción entre las proteínas priónicas en su forma anormal y la proteína priónica celular normal. Esta interacción conduce a la propagación de eventos de mal plegamiento a través de cambios conformacionales que resultan en la acumulación de agregados insolubles.
La agregación es un paso crítico en la patogénesis de los priones, ya que permite la propagación eficiente de proteínas mal plegadas en todo el sistema nervioso de un organismo. Estas estructuras agregadas son altamente resistentes a la degradación proteolítica, lo que lleva a su acumulación con el tiempo y causa trastornos neurodegenerativos como la enfermedad de Creutzfeldt-Jakob (ECJ) o la enfermedad de las vacas locas.
Comprender los mecanismos moleculares subyacentes a la agregación de priones puede proporcionar nuevas ideas sobre estrategias terapéuticas destinadas a prevenir o frenar el desarrollo de estas enfermedades. En particular, explorar formas de interrumpir el proceso de agregación podría conducir potencialmente a tratamientos efectivos para estas condiciones actualmente incurables.
La resistencia a los métodos de esterilización tradicionales es otro desafío planteado por los priones; este problema se abordará en secciones posteriores.
Resistencia a los métodos de esterilización tradicionales.
La resistencia de las proteínas priónicas a los métodos tradicionales de esterilización representa un desafío significativo para prevenir su propagación y transmisión. Los priones pueden resistir altas temperaturas, radiación y tratamientos químicos que son efectivos contra otros microorganismos. Esta capacidad se debe a la estructura única de las proteínas priónicas, que son altamente estables y resistentes a la desnaturalización.
El impacto de esta resistencia en la atención médica es significativo, ya que los priones pueden sobrevivir en equipos médicos, instrumentos quirúrgicos y superficies incluso después de los procedimientos de limpieza de rutina. Esto aumenta el riesgo de transmisión a través de productos sanguíneos contaminados o trasplantes de tejidos. El desarrollo de nuevos métodos de esterilización que apunten específicamente a los priones es crucial para reducir el riesgo de infección.
La resistencia de las proteínas priónicas a los métodos tradicionales de esterilización representa una grave amenaza para la salud pública. Es esencial desarrollar nuevas técnicas que puedan eliminar eficazmente estos agentes infecciosos de equipos médicos y otras superficies. Se deben implementar medidas de prevención y control para minimizar la exposición y reducir la propagación de enfermedades priónicas en entornos de atención médica.
Medidas de prevención y control
Para garantizar la prevención y el control de las enfermedades priónicas, deben implementarse regulaciones y directrices estrictas. Esto incluye la vigilancia y el seguimiento para detectar posibles brotes o nuevos casos. Además, se deben seguir estrictas directrices para la manipulación, eliminación y esterilización de materiales potencialmente contaminados con priones. Estas medidas son cruciales para mitigar los riesgos que representan estas amenazas silenciosas para la salud pública.
Vigilancia y monitoreo
La vigilancia y el monitoreo efectivos de las proteínas priónicas son cruciales para comprender sus posibles riesgos y desarrollar intervenciones para mitigar su impacto en la salud pública. Para lograr esto, el análisis de datos desempeña un papel crítico en la identificación de patrones de enfermedades priónicas, incluidas las tasas de incidencia, la distribución y las vías de transmisión.
La evaluación de riesgos también es esencial para determinar la probabilidad de exposición humana a los priones a través de diversas fuentes como alimentos contaminados, equipos médicos o accidentes de laboratorio. Los sistemas de vigilancia deben diseñarse para detectar señales de advertencia temprana de patologías priónicas mediante el uso de herramientas y técnicas de diagnóstico sensibles.
Los esfuerzos de vigilancia y monitoreo deben ser continuos para realizar un seguimiento de cualquier cambio en la prevalencia o distribución de las enfermedades priónicas con el tiempo. Esto requiere una estrecha colaboración entre diferentes partes interesadas involucradas en la salud pública, incluidos investigadores, médicos, agencias reguladoras y responsables políticos.
La información recopilada a partir de estos esfuerzos puede informar el desarrollo de medidas de prevención y control para infecciones por priones. En la sección posterior sobre 'regulaciones y pautas estrictas', discutiremos cómo se pueden implementar estas medidas de manera efectiva para evitar brotes de enfermedades priónicas.
Regulaciones y pautas estrictas.
Marco regulatorio y directrices rigurosas son necesarias para mitigar los posibles riesgos que presentan las enfermedades priónicas, ya que pueden servir como medios efectivos para prevenir y controlar brotes. La importancia de estas medidas se destaca por el hecho de que las enfermedades priónicas no tienen cura ni tratamiento conocido, lo que hace que la prevención sea la única opción viable.
La implementación de estas regulaciones involucra diversos aspectos, como la vigilancia y monitoreo de la alimentación animal, el movimiento del ganado y la prueba de animales para detectar enfermedades priónicas antes del sacrificio.
La implementación de estrictas regulaciones también incluye medidas para evitar que materiales contaminados entren en la cadena alimentaria, como la prohibición de ciertos tejidos de alto riesgo para su uso en la alimentación animal. Además, se establecen directrices para la correcta eliminación de materiales potencialmente infectados para limitar la exposición a humanos y otros animales.
Asegurar el cumplimiento de estas regulaciones es crucial para mitigar la propagación de enfermedades priónicas y proteger la salud pública. Con esta comprensión, queda claro que los marcos regulatorios y directrices estrictas son esenciales para abordar los posibles peligros que presentan las proteínas priónicas.
En cuanto a la investigación actual y las direcciones futuras, estudios recientes han mostrado resultados prometedores en el desarrollo de métodos de detección temprana para enfermedades priónicas a través de tecnologías innovadoras como la amplificación cíclica de mal plegamiento de proteínas (PMCA) y la conversión inducida por temblores en tiempo real (RT-QuIC). Estos avances podrían mejorar significativamente nuestra capacidad para detectar infecciones más temprano, permitiéndonos tomar medidas preventivas de manera más efectiva.
Investigación actual y direcciones futuras
La investigación reciente sobre las proteínas priónicas ha arrojado luz sobre su potencial para causar enfermedades neurodegenerativas, destacando la necesidad de seguir investigando sus mecanismos de acción e intervenciones terapéuticas posibles.
Las enfermedades priónicas son causadas por el mal plegamiento de una proteína celular normal, lo que conduce a la formación de proteínas priónicas anormales que pueden agregarse y acumularse en el cerebro. Estos agregados causan daño a las neuronas y, en última instancia, conducen a síntomas como demencia, pérdida de coordinación y dificultad para caminar.
La investigación actual se centra en comprender cómo los priones se propagan por todo el cerebro e identificar posibles objetivos para la intervención terapéutica. Una vía prometedora es el desarrollo de nuevos medicamentos que puedan prevenir la agregación de priones o promover la eliminación de proteínas agregadas. Además, se está trabajando para identificar biomarcadores que puedan ayudar en el diagnóstico temprano y el seguimiento de la progresión de la enfermedad.
Si bien todavía hay mucho por aprender sobre la prevención y el tratamiento de las enfermedades priónicas, los avances en nuestra comprensión de estos trastornos complejos ofrecen esperanza para futuras terapias. La investigación continua sobre los mecanismos subyacentes a la propagación de los priones será fundamental para desarrollar tratamientos efectivos que puedan detener o revertir la progresión de la enfermedad.
En última instancia, este trabajo podría conducir a nuevas estrategias terapéuticas no solo para las enfermedades priónicas, sino también para otros trastornos neurodegenerativos caracterizados por el mal plegamiento y la agregación de proteínas.
Preguntas frecuentes
¿Cuál es la historia de la investigación y el descubrimiento de los priones?
Irónicamente, el descubrimiento de priones no fue intencional, ni siquiera se consideraba posible su existencia hasta que se demostró. La investigación y los avances en priones han sido moldeados por una rica historia que incluye descubrimientos clave y figuras notables.
En los años 60, Stanley Prusiner introdujo el concepto de proteínas infecciosas como causa de scrapie en ovejas, lo que llevó a investigaciones sobre encefalopatías espongiformes transmisibles (EET) en animales y humanos. El descubrimiento de agentes infecciosos compuestos solo por proteínas desafió las opiniones convencionales sobre los virus y las bacterias como las únicas causas de infecciones.
Desde entonces, la investigación en priones ha logrado avances significativos en la comprensión de cómo se propagan estas proteínas y causan enfermedades, pero aún se desconoce mucho sobre sus mecanismos. Sin embargo, este campo continúa evolucionando con investigaciones en curso sobre nuevas técnicas de diagnóstico y posibles tratamientos para enfermedades priónicas como la enfermedad de Creutzfeldt-Jakob (ECJ).
¿Las enfermedades por priones se pueden transmitir de animales a humanos?
Las enfermedades priónicas son causadas por proteínas mal plegadas que pueden provocar daño cerebral y, en última instancia, la muerte. Si bien las enfermedades priónicas en humanos suelen adquirirse a través de mutaciones genéticas o exposición a equipo médico contaminado, existe preocupación por la transmisión animal y el potencial riesgo zoonótico.
La evidencia muestra que ciertas especies animales, como las vacas con encefalopatía espongiforme bovina (EEB), también conocida como "enfermedad de las vacas locas", han transmitido enfermedades priónicas a los humanos a través del consumo de carne contaminada. Además, estudios de laboratorio han demostrado que otros animales, como ratones y monos, pueden infectarse con priones de especies diferentes.
Aunque es raro, es importante que los investigadores continúen estudiando el potencial de transmisión animal a humano de las enfermedades priónicas para prevenir futuros brotes y proteger la salud pública.
¿Cómo afectan las proteínas priónicas al cerebro y al sistema nervioso?
La transmisión de la proteína priónica es un proceso complejo que puede tener efectos devastadores en el cerebro y el sistema nervioso. La estructura de la proteína priónica, que consiste en un plegamiento anormal, es responsable de su capacidad para transmitir enfermedades.
Una vez introducidas en un organismo, las proteínas priónicas se replican induciendo a las proteínas normales a adoptar su estado mal plegado, lo que conduce a la acumulación y aglomeración en el tejido cerebral. Esto puede provocar una serie de trastornos neurodegenerativos como la enfermedad de Creutzfeldt-Jakob (ECJ) y la variante de la ECJ (vECJ).
Un ejemplo del impacto de las enfermedades priónicas en los humanos es el brote de vECJ que ocurrió en el Reino Unido durante la década de 1990 debido al consumo de productos cárnicos contaminados. Si bien son raros, estos casos destacan la importancia de comprender cómo funcionan y se propagan las proteínas priónicas para que se puedan implementar medidas efectivas de prevención.
¿Existen tratamientos conocidos para las enfermedades por priones?
Las enfermedades por priones son un grupo de trastornos neurodegenerativos raros y mortales que afectan a humanos y otros animales. Actualmente, no se conocen tratamientos para estas enfermedades, lo que las hace particularmente peligrosas.
Sin embargo, los avances en la investigación han llevado a la identificación de posibles tratamientos para las enfermedades por priones. Un enfoque prometedor es el uso de moléculas pequeñas como terapias que pueden interferir en la agregación y propagación de proteínas de priones. Otra línea de investigación involucra la inmunoterapia, que utiliza anticuerpos para dirigirse y eliminar proteínas de priones anormales del cerebro.
Si bien estos posibles tratamientos muestran promesa en estudios preclínicos, todavía no han sido probados en ensayos clínicos. A pesar de los desafíos por delante, la investigación continua sobre las enfermedades por priones tiene una gran importancia para la salud pública dada su naturaleza mortal y la falta de opciones de tratamiento efectivas.
¿Cómo se diferencian las enfermedades priónicas de otras enfermedades neurodegenerativas, como el Alzheimer o el Parkinson?
Las enfermedades priónicas, como la enfermedad de Creutzfeldt-Jakob y la enfermedad de Creutzfeldt-Jakob variante, son únicas entre las enfermedades neurodegenerativas en que son causadas por una proteína mal plegada en lugar de una mutación genética o un factor ambiental.
Esta proteína, conocida como proteína priónica, puede volverse infecciosa y propagarse por todo el cerebro, lo que lleva a graves daños neurológicos y la muerte.
Si bien no hay cura conocida para las enfermedades priónicas, la investigación reciente se ha centrado en identificar predisposiciones genéticas a estos trastornos para desarrollar medidas preventivas.
Además, comprender el proceso de plegamiento incorrecto de proteínas puede ofrecer pistas para desarrollar tratamientos no solo para enfermedades priónicas, sino también para otros trastornos neurodegenerativos como el Alzheimer y el Parkinson.
Conclusión
Las proteínas priónicas son una amenaza silenciosa que puede causar enfermedades fatales en humanos y animales. Estas proteínas son únicas en su capacidad para auto-replicarse, causando una cascada de eventos de plegamiento incorrecto que llevan a trastornos neurodegenerativos como la enfermedad de Creutzfeldt-Jakob y la enfermedad de las vacas locas. El peligro radica en el hecho de que los priones pueden transmitirse a través de alimentos, transfusiones de sangre y equipos quirúrgicos contaminados.
Los priones mal plegados exhiben resistencia a los métodos tradicionales de esterilización, lo que dificulta a los proveedores de atención médica eliminarlos de los instrumentos médicos. Además, los síntomas de las enfermedades priónicas a menudo se confunden con otras condiciones, lo que lleva a diagnósticos tardíos y opciones de tratamiento inadecuadas.
Un ejemplo de los efectos devastadores de las enfermedades priónicas es el brote de la enfermedad de las vacas locas en el Reino Unido durante la década de 1990. Esta epidemia causó pánico generalizado entre los consumidores y llevó a pérdidas económicas significativas para los agricultores y procesadores de carne. También destacó la necesidad de medidas más estrictas para prevenir y controlar las infecciones priónicas.
Los esfuerzos actuales de investigación se centran en desarrollar nuevas herramientas de diagnóstico y tratamientos terapéuticos contra las enfermedades priónicas. Sin embargo, queda mucho trabajo por hacer para comprender los complejos mecanismos subyacentes del plegamiento incorrecto de proteínas y la propagación.
Con esfuerzos continuos de científicos, responsables políticos y profesionales de la salud, algún día podremos conquistar esta amenaza silenciosa de una vez por todas.
Si quieres conocer otros artículos parecidos a ¿Por qué las proteínas prion son peligrosas? - La amenaza silenciosa. puedes visitar la categoría Bioquímica.
Deja una respuesta



¡Más Contenido!