
¿Para qué sirven las proteínas de choque térmico? - Los bomberos de nuestras células.
Las proteínas de choque térmico (HSP, por sus siglas en inglés) son una familia de moléculas altamente conservadas que se encuentran en todas las células vivas. Fueron descubiertas originalmente en la década de 1960 como respuesta al estrés térmico, de ahí su nombre.
Sin embargo, ahora se sabe que estas proteínas desempeñan roles críticos en muchos procesos celulares más allá del choque térmico. Las HSP también están involucradas en el plegamiento, transporte y degradación de proteínas, así como en la señalización celular y las respuestas inmunitarias.
A pesar de su importancia, las HSP siguen siendo relativamente desconocidas fuera de los círculos científicos. Este artículo tiene como objetivo arrojar luz sobre las funciones de las HSP y por qué a menudo se les llama los 'bomberos' o 'bomberos' de nuestras células.
Discutiremos cómo se producen y regulan estas proteínas, los diferentes tipos de HSP que existen y su papel en diversas enfermedades. Además, exploraremos cómo los investigadores están utilizando el conocimiento sobre las HSP para desarrollar nuevos enfoques terapéuticos para tratar enfermedades como el cáncer y los trastornos neurodegenerativos.
- Introducción a las Proteínas de Choque Térmico (HSP)
- Producción de HSPs
- Tipos de HSPs
- Papel de las HSPs en la enfermedad.
- HSPs como objetivos terapéuticos
-
Preguntas frecuentes
- ¿Cuál es la estructura de las proteínas de choque térmico y cómo contribuye a su función?
- ¿Cómo afectan los factores ambientales como la temperatura y los estresores a la producción de HSP en las células?
- ¿Existen enfermedades o condiciones específicamente relacionadas con la deficiencia de HSPs?
- ¿Cuáles son algunos posibles efectos secundarios o desventajas de utilizar HSP como objetivos terapéuticos en la medicina?
- ¿Existen otros mecanismos celulares o proteínas que trabajen en conjunto con las HSP para proteger las células del estrés y el daño?
- Conclusión
Introducción a las Proteínas de Choque Térmico (HSP)
La función de las Proteínas de Choque Térmico (HSP, por sus siglas en inglés) implica su papel como chaperonas moleculares en ayudar al plegamiento, ensamblaje y estabilización de proteínas bajo condiciones de estrés celular. Las HSP son importantes porque ayudan a proteger las células de los efectos dañinos de factores estresantes ambientales como altas temperaturas, estrés oxidativo y exposición a toxinas.
Estas proteínas desempeñan un papel fundamental en asegurar el correcto plegamiento de proteínas y prevenir que proteínas mal plegadas o agregadas se acumulen dentro de las células. Las proteínas son moléculas esenciales que llevan a cabo muchas funciones críticas dentro de las células.
Sin embargo, cuando se exponen a factores estresantes ambientales, las proteínas pueden dañarse o plegarse de manera incorrecta, lo que lleva a la formación de agregados disfuncionales que pueden ser tóxicos para las células.
Las HSP ayudan a prevenir este daño uniéndose a proteínas desplegadas o parcialmente plegadas y facilitando su correcto plegamiento en estructuras funcionales. También trabajan estabilizando proteínas durante momentos de estrés celular. Las HSP han sido implicadas en una variedad de procesos biológicos, incluyendo el envejecimiento, la inmunidad, la progresión del cáncer y las enfermedades neurodegenerativas.
En algunos casos, se ha demostrado que actúan como potentes reguladores de las vías de señalización celular involucradas en la inflamación y la apoptosis. La investigación ha demostrado que las mutaciones en los genes que codifican para las HSP pueden llevar al desarrollo de ciertas enfermedades.
Las Proteínas de Choque Térmico desempeñan un papel importante en mantener la salud celular bajo condiciones de estrés al actuar como chaperonas moleculares para el correcto plegamiento y estabilidad de proteínas.
Sus diversas funciones las convierten en componentes críticos para los procesos celulares normales y sin ellas, las células no podrían hacer frente a diversos tipos de estrés ambiental. Comprender la importancia de estas moléculas notables es crucial para desarrollar terapias efectivas contra estados de enfermedad asociados con la función o agregación de proteínas inadecuadas, como el cáncer o la neurodegeneración.
Producción de HSPs
Producir proteínas de choque térmico (HSP) es una respuesta común a los estresores celulares. Estas proteínas son cruciales para mantener la homeostasis celular durante momentos de estrés ambiental o fisiológico, como temperaturas elevadas, estrés oxidativo y exposición a toxinas. El mecanismo de producción de HSP implica una serie compleja de eventos que resultan en la regulación al alza de genes que codifican estas proteínas.
El primer paso en la producción de HSP es la activación de factores de transcripción que se unen a regiones específicas de ADN conocidas como elementos de choque térmico (HSE). Esta unión resulta en el reclutamiento de la ARN polimerasa y la posterior transcripción de los genes HSP.
Una vez transcritas, estas moléculas de ARNm se traducen en sus respectivos productos proteicos por los ribosomas. Los chaperones luego ayudan con el plegamiento adecuado de las proteínas y su transporte a sus ubicaciones subcelulares apropiadas.
La función de HSP en la respuesta al estrés celular es multifacética y depende de la proteína específica involucrada. Algunas HSP actúan como chaperonas moleculares, previniendo que las proteínas mal plegadas o desnaturalizadas se agreguen y ayudando en su replegamiento.
Otros facilitan la degradación proteosómica de proteínas dañadas o participan en mecanismos de eliminación mediados por autofagia. Además, algunas HSP han sido implicadas en vías de señalización que activan otros mecanismos de respuesta al estrés.
Para comprender mejor el papel que desempeñan las HSP durante los estresores celulares, puede ser útil considerar la siguiente tabla:
| Estresor | Proteínas de choque térmico reguladas al alza | Función |
|---|---|---|
| Temperaturas elevadas | Hsp70, Hsp90 | Plegamiento de proteínas / chaperona |
| Estrés oxidativo | Hsp27 | Prevenir la agregación |
| Grp78/BiP | Facilitar la degradación | |
| Exposición a toxinas | Grp94 | Plegamiento de proteínas / chaperona |
| ClpB/Hsp104 | Desagregación / reparación de agregados |
La producción de HSP es un mecanismo fundamental mediante el cual las células responden a los estresores. Estas proteínas desempeñan roles críticos en el mantenimiento de la homeostasis celular y la prevención del daño causado por el estrés ambiental y fisiológico. Comprender los mecanismos complejos involucrados en su producción y función puede proporcionar información valiosa sobre cómo podemos proteger mejor las células de los estresores dañinos.
Tipos de HSPs
Una forma de conceptualizar la diversidad de las proteínas de choque térmico (HSPs) es pensar en ellas como una caja de herramientas, cada una con su función y propósito único, que las células pueden utilizar en respuesta a diferentes factores de estrés.
Las HSPs se clasifican en diferentes grupos según su peso molecular, incluyendo las pequeñas HSPs (sHSPs), la familia Hsp60, la familia Hsp70 y la familia Hsp90. Cada grupo tiene una estructura distinta y desempeña un papel esencial en la homeostasis celular.
Las pequeñas HSPs actúan como chaperonas al unirse a proteínas desnaturalizadas y evitar que se agreguen o sufran una mayor degradación. Estas sHSPs ayudan a estabilizar las estructuras proteicas en condiciones de estrés como el choque térmico o el estrés oxidativo.
La familia Hsp60 ayuda en el plegamiento de proteínas dentro de las mitocondrias al formar complejos en forma de barril alrededor de polipéptidos desplegados. En contraste, la familia Hsp70 ayuda a replegar proteínas mal plegadas al unirse a regiones hidrofóbicas expuestas de estas moléculas y promover el plegamiento dependiente de ATP.
El grupo más grande de HSPs es la familia Hsp90, que desempeña roles críticos en la regulación de la actividad proteica a través de interacciones con co-chaperonas. Ayudan en el plegamiento de nuevas cinasas y receptores de hormonas esteroides, mientras estabilizan estas moléculas durante cambios conformacionales. Además, ayudan a degradar proteínas dañadas al interactuar con ligasas de ubiquitina.
La regulación de la expresión de hsps ocurre en múltiples niveles que van desde el control transcripcional por factores de transcripción específicos como el factor de choque térmico 1 (HSF1) hasta las modificaciones post-transcripcionales como la fosforilación o acetilación que modulan su estabilidad y actividad. La disregulación de las hsps puede resultar en diversas enfermedades como el cáncer o la neurodegeneración.
Comprender las funciones y la regulación de las hsps es crucial para desarrollar intervenciones terapéuticas para diversas enfermedades asociadas con el mal plegamiento o la agregación de proteínas. Los diversos roles desempeñados por los diferentes miembros de esta caja de herramientas proteica resaltan su importancia en el mantenimiento de la homeostasis celular y la adaptación a condiciones de estrés.

Papel de las HSPs en la enfermedad.
El papel de las proteínas de choque térmico (HSPs) en varias enfermedades ha sido ampliamente estudiado y documentado. En enfermedades neurodegenerativas como el Alzheimer y el Parkinson, se ha demostrado que las HSPs desempeñan un papel protector al prevenir la agregación de proteínas y ayudar en la eliminación de proteínas dañadas.
En el cáncer, se sabe que las HSPs promueven el crecimiento y la supervivencia de los tumores al inhibir la apoptosis y promover la metástasis. Finalmente, en las enfermedades cardiovasculares, las HSPs han sido implicadas en roles protectores y patológicos dependiendo del estado de la enfermedad específica y del contexto.
En general, comprender la participación de las HSPs en la patogénesis de las enfermedades puede conducir a nuevos enfoques terapéuticos para estas condiciones.
Enfermedades neurodegenerativas
Las enfermedades neurodegenerativas, como el Alzheimer y el Parkinson, han sido relacionadas con la disfunción de las proteínas de choque térmico (HSPs). Estas proteínas son responsables de reparar proteínas dañadas o mal plegadas dentro de las células. Cuando las HSPs no funcionan correctamente, puede conducir a un plegamiento y agregación de proteínas, lo cual son características clave de las enfermedades neurodegenerativas.
Las consecuencias de estas anormalidades en las proteínas en las enfermedades neurodegenerativas pueden ser devastadoras.
Aquí hay tres ejemplos:
- En la enfermedad de Alzheimer, los péptidos beta amiloides se agregan en placas que interrumpen la comunicación neuronal y llevan a una disminución cognitiva;
- En la enfermedad de Parkinson, las proteínas alfa-sinucleína se pliegan de manera incorrecta y forman cuerpos de Lewy que dañan las neuronas en el tronco cerebral;
- En la enfermedad de Huntington, las proteínas huntingtina se acumulan en el cerebro y causan una deterioración progresiva de la función motora y cognitiva.
Entender el papel de las HSPs en la prevención de estas anormalidades en las proteínas es crucial para el desarrollo de tratamientos efectivos para estas enfermedades devastadoras.
Cáncer
Similar a como un guardia vigilante protege la seguridad de una comunidad, entender el papel de las proteínas de choque térmico en la regulación del crecimiento y muerte celular es fundamental en el desarrollo de tratamientos efectivos contra el cáncer.
Las proteínas de choque térmico (HSP, por sus siglas en inglés) son un grupo de chaperonas moleculares que ayudan a las células a sobrevivir en condiciones estresantes como altas temperaturas, hipoxia y estrés oxidativo. Las HSP también desempeñan un papel importante en el desarrollo y progresión del cáncer.
En las células cancerosas, las HSP se sobreexpresan como un mecanismo de protección contra la quimioterapia y la radioterapia. Al inhibir la función de las HSP, es posible sensibilizar las células cancerosas a estas terapias.
Por lo tanto, los investigadores están explorando el uso de inhibidores de HSP como posibles medicamentos para mejorar la eficacia del tratamiento del cáncer. Actualmente se están llevando a cabo varios ensayos clínicos para evaluar la seguridad y eficacia de varios inhibidores de HSP solos o en combinación con regímenes estándar de quimioterapia o inmunoterapia.
Entender los complejos roles desempeñados por las HSP en la biología del cáncer puede llevar a enfoques terapéuticos novedosos para mejorar los resultados de los pacientes.
Enfermedades Cardiovasculares
Las enfermedades cardiovasculares son una preocupación importante para la salud pública, representando un porcentaje significativo de las muertes globales cada año. Estas enfermedades afectan al corazón y los vasos sanguíneos, lo que puede llevar a complicaciones como infartos, accidentes cerebrovasculares y enfermedad arterial periférica.
Los factores de riesgo para las enfermedades cardiovasculares incluyen la hipertensión, el tabaquismo, la obesidad, la diabetes mellitus, la inactividad física y una dieta poco saludable. Las estrategias de prevención para las enfermedades cardiovasculares implican modificar el estilo de vida para abordar estos factores de riesgo.
Por ejemplo, mantener un peso saludable a través de ejercicio regular y una nutrición equilibrada puede reducir la probabilidad de desarrollar hipertensión o diabetes tipo 2. La cesación del tabaquismo también es fundamental para reducir el riesgo de enfermedades cardíacas y accidentes cerebrovasculares.
Además, controlar los niveles de estrés a través de técnicas de relajación puede ayudar a reducir la presión arterial y promover el bienestar general. Otras estrategias de prevención pueden incluir el manejo de medicamentos para aquellos que ya han sido diagnosticados con hipertensión o diabetes para prevenir complicaciones adicionales.
Al implementar estas medidas desde temprana edad y monitorear constantemente el estado de salud a través de chequeos regulares con proveedores de atención médica, las personas pueden reducir significativamente sus posibilidades de desarrollar enfermedades cardiovasculares más adelante en la vida.
HSPs como objetivos terapéuticos
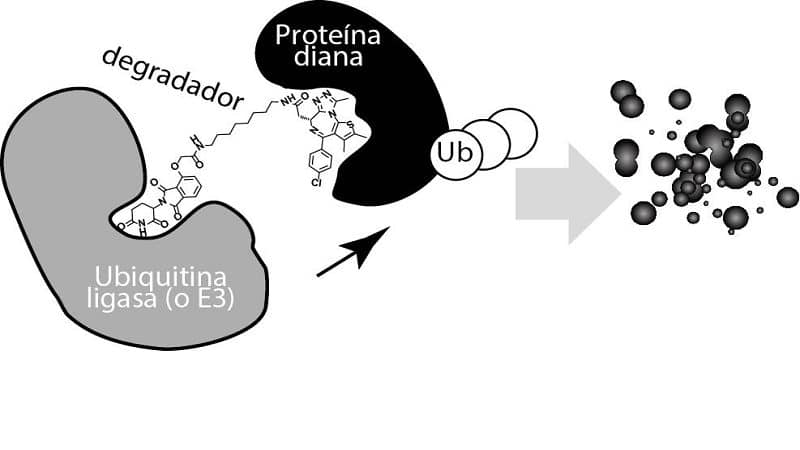
Una aplicación potencial de las HSP es en el desarrollo de objetivos terapéuticos para una variedad de enfermedades y condiciones. Se ha demostrado que las HSP están involucradas en varios procesos celulares, incluyendo el plegamiento, ensamblaje y degradación de proteínas. Como tal, desempeñan un papel crucial en el mantenimiento de la homeostasis celular en condiciones de estrés.
Las siguientes son algunas posibles implicaciones clínicas del uso de las HSP como objetivos terapéuticos:
- Cáncer: Las células tumorales a menudo dependen de la activación de las HSP para garantizar su supervivencia y proliferación. La orientación de estas proteínas puede conducir a la muerte de las células cancerosas o a la sensibilización a otras terapias.
- Enfermedades neurodegenerativas: Las proteínas mal plegadas son una característica distintiva de enfermedades neurodegenerativas como la enfermedad de Alzheimer y la enfermedad de Parkinson. Las HSP pueden ayudar a prevenir el plegamiento y la agregación de proteínas, lo que las convierte en objetivos prometedores para el desarrollo de fármacos.
- Enfermedades cardiovasculares: Como se discutió anteriormente, las HSP pueden proteger contra el daño cardiovascular al reducir la inflamación y prevenir la muerte celular. Al dirigirse a estas proteínas, puede ser posible desarrollar nuevos tratamientos para enfermedades cardíacas.
Si bien aún se necesita mucha investigación antes de que las terapias basadas en HSP se conviertan en una realidad, estos hallazgos demuestran las posibles aplicaciones clínicas de la orientación de estas proteínas esenciales. Los estudios actuales sugieren que modular la actividad de ciertos tipos de HSP puede proporcionar beneficios en varios campos médicos diferentes.
Aunque nuestra comprensión de la función completa de las HSP aún se está desarrollando, hay una promesa significativa en el uso de ellas como objetivos terapéuticos en una variedad de entornos. Con más investigación sobre sus mecanismos e interacciones con otros componentes celulares, pronto podríamos ver nuevos fármacos desarrollados que se dirijan a tipos específicos de HSP para tratar muchos tipos diferentes de enfermedades y trastornos.
Preguntas frecuentes
¿Cuál es la estructura de las proteínas de choque térmico y cómo contribuye a su función?
Las proteínas de choque térmico (HSPs) son chaperonas moleculares que desempeñan un papel crucial en el mantenimiento de la homeostasis celular en condiciones de estrés. Estas proteínas son altamente conservadas y han sido identificadas en todos los organismos vivos, desde bacterias hasta humanos.
La estructura de las HSPs se caracteriza por su capacidad para adoptar diferentes conformaciones, lo que les permite interactuar con varias proteínas cliente. La arquitectura típica de las HSPs consta de dos dominios: un dominio N-terminal que contiene la actividad de ATPasa y un dominio C-terminal responsable de la unión del sustrato.
La actividad de ATPasa es esencial para la actividad de chaperona de las HSPs, ya que proporciona la energía necesaria para los procesos de plegamiento y desplegamiento de proteínas. Además, las HSPs pueden formar grandes complejos oligoméricos que facilitan el replegamiento de proteínas y evitan la agregación durante el estrés térmico.
Las características estructurales únicas de las HSPs les permiten funcionar como chaperonas moleculares y proteger las células contra el estrés proteotóxico causado por estímulos ambientales como el calor o el daño oxidativo.
¿Cómo afectan los factores ambientales como la temperatura y los estresores a la producción de HSP en las células?
La regulación ambiental desempeña un papel crucial en la formación de la respuesta celular a los factores estresantes como los cambios de temperatura. Las proteínas de choque térmico (HSPs) son una clase de chaperonas moleculares que se inducen por estímulos ambientales y funcionan para proteger a las células de diversas formas de estrés, incluyendo el calor, el daño oxidativo y la exposición a metales pesados.
La producción de HSPs está estrechamente regulada a través de una compleja red de vías de señalización que involucran varios factores de transcripción y co-chaperonas. Específicamente, la respuesta al choque térmico se inicia cuando las proteínas mal plegadas o desnaturalizadas se acumulan en la célula debido a factores estresantes ambientales. Esto conduce a la activación de factores de transcripción como HSF1, que aumenta la expresión de genes HSP.
Los factores ambientales como la temperatura y los factores estresantes juegan un papel importante en la modulación de las respuestas celulares mediadas por HSPs, lo que en última instancia ayuda a mantener la homeostasis proteica y prevenir la muerte celular en condiciones adversas.
¿Existen enfermedades o condiciones específicamente relacionadas con la deficiencia de HSPs?
La ausencia de proteínas de choque térmico (HSP) en el entorno celular ha sido relacionada con diversas enfermedades neurodegenerativas, incluyendo Parkinson y Alzheimer. Las HSP desempeñan un papel crucial en la prevención del plegamiento de proteínas y su agregación, una característica de estas enfermedades.
Además, la falta de HSP también permite el crecimiento y la proliferación ilimitados de células cancerosas, ya que son componentes esenciales del microentorno tumoral. Sin embargo, la sobreexpresión o activación de las HSP puede ser aprovechada terapéuticamente para dirigirse selectivamente a las células cancerosas mientras se preserva la función normal del tejido.
Estos hallazgos sugieren que mantener niveles adecuados de expresión de HSP es crítico para la prevención y el tratamiento de enfermedades. En esencia, las HSP pueden ser consideradas como bomberos celulares que protegen contra incendios patológicos como el plegamiento de proteínas y la progresión del cáncer.
¿Cuáles son algunos posibles efectos secundarios o desventajas de utilizar HSP como objetivos terapéuticos en la medicina?
Posibles efectos secundarios o desventajas de utilizar HSP como objetivos terapéuticos en medicina podrían incluir preocupaciones éticas en torno al uso de estas proteínas y su impacto potencial en células sanas.
Aunque HSP ha demostrado promesas en el tratamiento del cáncer, dirigirse a ellas también puede llevar a consecuencias no deseadas como un aumento en la resistencia a la quimioterapia o radioterapia.
Además, existe el riesgo de que dirigirse a HSP pueda resultar en la supresión de funciones celulares normales, lo que lleva a efectos adversos en la salud general.
A pesar de estos riesgos potenciales, la investigación sobre el uso de HSP como objetivos terapéuticos continúa, con esfuerzos en curso dirigidos a identificar formas de minimizar cualquier impacto negativo asociado con su uso.
En última instancia, se necesita más estudio para comprender completamente tanto los beneficios como los riesgos asociados con el uso de HSP como forma de tratamiento médico.
¿Existen otros mecanismos celulares o proteínas que trabajen en conjunto con las HSP para proteger las células del estrés y el daño?
Los mecanismos celulares y las proteínas trabajan en conjunto con las HSP para proteger las células del estrés y daño.
El papel de las HSP en el tratamiento del cáncer ha sido ampliamente estudiado, ya que juegan un papel importante en la supervivencia de las células cancerosas y la resistencia a la terapia.
Además, la interacción entre las HSP y la respuesta del sistema inmunológico es crucial para mantener la homeostasis celular en condiciones de estrés.
Investigaciones recientes sugieren que las HSP pueden regular las respuestas inflamatorias mediante la modulación de la función de las células inmunológicas y la producción de citoquinas.
Además, otros chaperones moleculares como GRP78/BiP han demostrado inhibir la apoptosis y promover la supervivencia celular durante el estrés del retículo endoplásmico.
Por lo tanto, comprender la compleja red de proteínas involucradas en la protección celular proporcionará información valiosa para desarrollar nuevas estrategias terapéuticas para diversas enfermedades, incluyendo el cáncer.
Conclusión
Las proteínas de choque térmico (HSP) son un grupo de moléculas altamente conservadas que desempeñan un papel esencial en la protección de las células contra el daño causado por factores estresantes como el calor, la radiación y las toxinas. Estas proteínas actúan como chaperonas moleculares, ayudando a mantener la integridad estructural de otras proteínas dentro de la célula.
Además de su función protectora, las HSP se han relacionado con diversas enfermedades, incluyendo el cáncer, trastornos neurodegenerativos y enfermedades autoinmunitarias. La investigación reciente se ha centrado en desarrollar estrategias terapéuticas que apunten a las HSP. Estos enfoques buscan inhibir o activar estas proteínas según la enfermedad específica que se esté tratando.
Por ejemplo, se ha demostrado que la inhibición de la expresión de HSP es efectiva contra ciertos tipos de cáncer, mientras que la activación de HSP puede ser beneficiosa para enfermedades neurodegenerativas. La versatilidad de estas moléculas las convierte en objetivos atractivos para la intervención terapéutica en una variedad de diferentes enfermedades.
Las HSP son jugadores críticos en la homeostasis celular y la patogénesis de enfermedades. La investigación continuada sobre los mecanismos subyacentes a la función de las HSP es probable que genere nuevas ideas sobre cómo estas moléculas contribuyen tanto a la salud como a la enfermedad.
Si quieres conocer otros artículos parecidos a ¿Para qué sirven las proteínas de choque térmico? - Los bomberos de nuestras células. puedes visitar la categoría Biología molecular.
Deja una respuesta




¡Más Contenido!