
¿Dónde se utiliza la biotecnología en la medicina? - Salvando vidas a nivel molecular.
La biotecnología es la aplicación de organismos vivos y sistemas biológicos para producir productos y procesos útiles. Ha revolucionado varios campos como la agricultura, la industria y la medicina.
En medicina, la biotecnología ha desempeñado un papel significativo no solo en mejorar el diagnóstico y tratamiento de enfermedades, sino también en el desarrollo de nuevas terapias que antes eran inimaginables. El uso de biotecnología en medicina implica la manipulación de células vivas y sus componentes para producir medicamentos novedosos o modificar los existentes.
En este artículo, exploraremos dónde se utiliza la biotecnología en la medicina - Salvando vidas a nivel molecular, explorando diferentes aplicaciones de la biotecnología en medicina como la producción de medicamentos biológicos, técnicas de diagnóstico, ingeniería de tejidos y medicina regenerativa.
- Introducción a la Biotecnología en Medicina.
- Producción de medicamentos biológicos.
- Técnicas de diagnóstico
- Ingeniería de Tejidos y Medicina Regenerativa
- Desafíos éticos y regulatorios
- Futuro de la Biotecnología en Medicina.
-
Preguntas frecuentes
- ¿Cuáles son algunos ejemplos específicos de medicamentos biológicos producidos a través de la biotecnología?
- ¿En qué se diferencia la ingeniería de tejidos de los métodos de trasplante tradicionales?
- ¿Cuáles son algunas preocupaciones éticas comunes en torno al uso de la biotecnología en la medicina?
- ¿Existen marcos regulatorios actuales para el uso de la biotecnología en la medicina?
- ¿Qué nuevos avances o desarrollos podemos esperar en el futuro de la biotecnología en la medicina?
- Conclusión
Introducción a la Biotecnología en Medicina.
La utilización de la biotecnología en medicina sirve como una introducción al estudio de intervenciones a nivel molecular que tienen como objetivo salvar vidas. La biotecnología se refiere a la aplicación de principios y técnicas científicas para manipular organismos vivos o sus componentes para uso humano, creando así nuevos productos y servicios.
En la medicina moderna, la biotecnología ha revolucionado la forma en que se diagnostican, tratan y previenen enfermedades.
Una de las aplicaciones de la biotecnología en la medicina moderna es la medicina personalizada. La medicina personalizada implica adaptar el tratamiento médico a la composición genética o a otras características únicas de un individuo. Este enfoque permite a los médicos prescribir tratamientos más efectivos con menos efectos secundarios.
La biotecnología también permite a los investigadores desarrollar vacunas contra enfermedades anteriormente incurables, como el cáncer y la enfermedad de Alzheimer.
Otro beneficio de la biotecnología en la medicina moderna es la terapia génica. La terapia génica implica insertar una copia sana de un gen defectuoso en las células de un paciente para reemplazarla por la defectuosa. Esta técnica ha demostrado ser prometedora en el tratamiento de trastornos genéticos hereditarios como la fibrosis quística y la anemia de células falciformes.
Finalmente, la biotecnología ha llevado a avances en la investigación de células madre, que implican el uso de células no diferenciadas que tienen el potencial de convertirse en cualquier tipo de tejido u órgano en el cuerpo.
Las células madre pueden utilizarse para terapias regenerativas para tejidos u órganos dañados, como los que se encuentran en la enfermedad de Parkinson y las lesiones de la médula espinal.
Producción de medicamentos biológicos.
Una aplicación importante de la biotecnología en medicina es la producción de medicamentos biológicos. Este proceso implica la síntesis biológica de fármacos conocidos como biotecnológicos. La fabricación de biotecnológicos es un proceso complejo y delicado que requiere un alto nivel de precisión y control para garantizar la seguridad, pureza y eficacia del producto final.
La producción de biotecnológicos involucra varias etapas, incluyendo el cultivo celular, la purificación, la formulación y el envasado. En la primera etapa, se utilizan células vivas para producir la proteína o molécula deseada que se utilizará como medicamento. Estas células se seleccionan cuidadosamente por su capacidad para producir altos rendimientos de la proteína objetivo mientras mantienen su estabilidad e integridad genética.
Una vez producida, la proteína debe ser purificada de otros componentes celulares utilizando diversas técnicas como la cromatografía o la filtración. La proteína purificada se formula en una forma de dosificación adecuada para la administración a los pacientes.
Finalmente, el medicamento envasado se somete a pruebas rigurosas para garantizar su seguridad y eficacia antes de que pueda ser aprobado para su uso por las agencias reguladoras.
Técnicas de diagnóstico
El campo de las técnicas de diagnóstico en medicina abarca una variedad de tecnologías y métodos. Tres áreas clave que han revolucionado el diagnóstico médico son la secuenciación de ADN, la imagenología médica y los dispositivos de atención médica en el punto de atención.
Estas herramientas permiten a los médicos identificar marcadores genéticos para enfermedades, visualizar estructuras dentro del cuerpo y obtener resultados de diagnóstico rápidos en la cama del paciente.
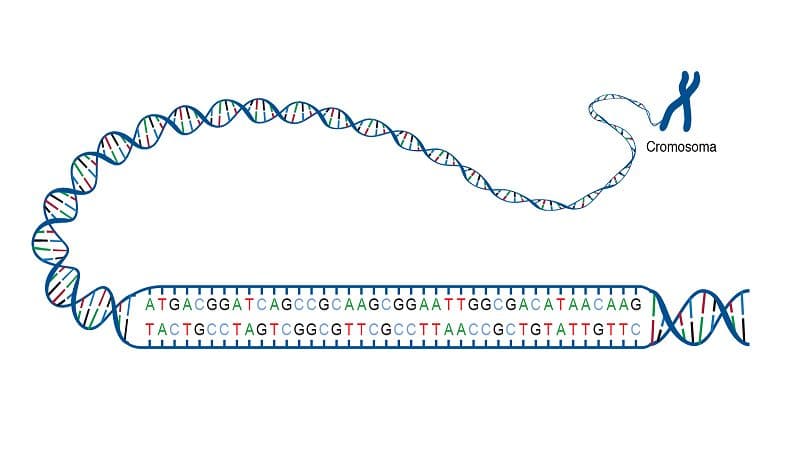
Secuenciación de ADN
La tecnología de secuenciación de ADN ha revolucionado el campo de la medicina, con un estimado de 20,000 genomas secuenciados por año en todo el mundo. Esto ha proporcionado conocimientos invaluables sobre el diagnóstico y tratamiento de enfermedades. Las aplicaciones de la secuenciación de ADN son vastas, y la medicina personalizada es una de sus implicaciones más prometedoras.
- Identificación de predisposiciones genéticas: La secuenciación de ADN permite la identificación de mutaciones genéticas que pueden predisponer a individuos a ciertas enfermedades o condiciones.
- Medicina de precisión: Al comprender la composición genética única de un paciente, los profesionales médicos pueden proporcionar tratamientos personalizados que son más efectivos que los enfoques tradicionales.
- Detección y prevención temprana: La secuenciación de ADN también puede ayudar en los esfuerzos de detección y prevención temprana, identificando a individuos de alto riesgo antes de que aparezcan los síntomas.
- Investigación de enfermedades: Finalmente, la secuenciación de ADN juega un papel crucial en la investigación de enfermedades al proporcionar a los científicos una mejor comprensión de la base molecular de varias enfermedades.
En general, la secuenciación de ADN ha tenido un impacto significativo en el campo de la medicina al permitir enfoques personalizados para el diagnóstico y tratamiento. A medida que la tecnología continúa avanzando, es probable que surjan aplicaciones aún más sofisticadas en el futuro.
Imagen médica
Las tecnologías de imágenes médicas proporcionan representaciones visuales de estructuras y procesos internos, ayudando en el diagnóstico y tratamiento de una amplia gama de condiciones médicas. Estas técnicas de diagnóstico por imágenes permiten a los profesionales de la salud ver dentro del cuerpo humano sin procedimientos invasivos, proporcionando información valiosa que puede guiar las decisiones de tratamiento.
Los avances en la imagenología médica han revolucionado la medicina, permitiendo una detección temprana de enfermedades, una mayor precisión en el diagnóstico y tratamientos más específicos.
Uno de los tipos más comunes de imágenes médicas es la tecnología de rayos X, que utiliza radiación electromagnética para crear imágenes de huesos y otros tejidos duros dentro del cuerpo. Otros tipos de diagnóstico por imágenes incluyen tomografías computarizadas (TC), imágenes de resonancia magnética (IRM), ultrasonido, escaneos de medicina nuclear y tomografías por emisión de positrones (PET).
Cada tipo tiene sus propias fortalezas y limitaciones dependiendo de la condición médica específica que se está evaluando. Por ejemplo, las tomografías computarizadas son particularmente útiles para identificar tumores o lesiones en órganos como el cerebro o los pulmones, mientras que la IRM es mejor para identificar anomalías en tejidos blandos como los encontrados en los músculos o tendones.
En general, estas tecnologías de imágenes médicas continúan evolucionando rápidamente con esfuerzos de investigación en curso destinados a mejorar su precisión y efectividad en el diagnóstico y tratamiento de enfermedades.
Dispositivos de Punto de Atención
Los dispositivos de atención médica son herramientas diagnósticas portátiles diseñadas para proporcionar resultados de pruebas inmediatas en la cabecera del paciente o en lugares remotos. Estos dispositivos han revolucionado la prestación de atención médica al mejorar el acceso a las pruebas médicas, especialmente en entornos con recursos limitados donde no está disponible la infraestructura de laboratorio tradicional.
Los dispositivos de atención médica utilizan una variedad de tecnologías, como biosensores, microfluidos y plataformas de laboratorio en un chip, para realizar pruebas en fluidos corporales como sangre, orina y saliva.
El desarrollo de dispositivos de atención médica presenta varios desafíos, como la miniaturización de la tecnología manteniendo una alta sensibilidad y especificidad, la integración con la tecnología de comunicación inalámbrica para la transferencia y almacenamiento de datos, garantizar la facilidad de uso para los profesionales médicos con capacitación mínima, el cumplimiento normativo y la estandarización de protocolos.
Sin embargo, a pesar de estos desafíos, también existen importantes oportunidades de mercado debido a la creciente demanda de opciones de diagnóstico y tratamiento más rápidas con una mayor precisión.
El mercado global de diagnóstico en el punto de atención se valoró en $18.5 mil millones en 2020 y se espera que crezca a una tasa compuesta anual del 7% en la próxima década impulsado por factores como el aumento de la prevalencia de enfermedades crónicas, la creciente conciencia sobre la detección temprana de enfermedades y los avances tecnológicos en técnicas de diagnóstico.
Ingeniería de Tejidos y Medicina Regenerativa
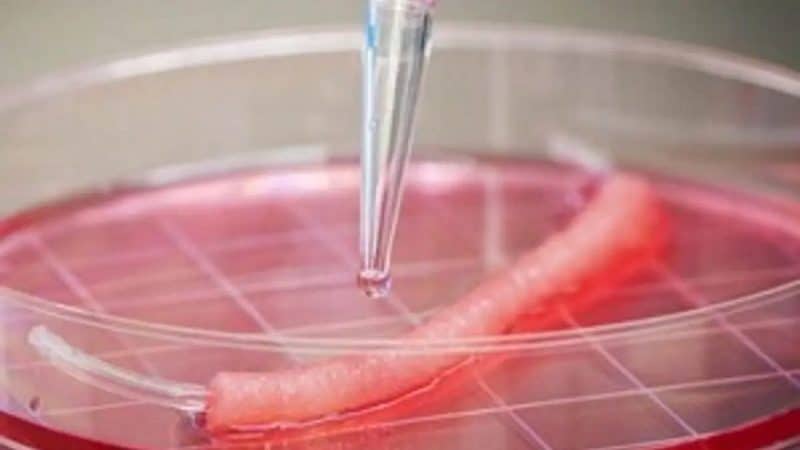
La ingeniería de tejidos y la medicina regenerativa han surgido como campos prometedores dentro de la biotecnología, ofreciendo soluciones innovadoras para reparar o reemplazar tejidos y órganos dañados en el cuerpo.
Las terapias regenerativas buscan estimular el proceso de curación mediante el uso de células madre y factores de crecimiento, mientras que la ingeniería de tejidos implica crear tejidos funcionales desde cero.
Ambos enfoques tienen un gran potencial para tratar una amplia gama de enfermedades y lesiones, como enfermedades cardíacas, diabetes, trastornos neurodegenerativos y lesiones de la médula espinal.
Uno de los principales desafíos en la ingeniería de tejidos es crear estructuras que imiten la compleja arquitectura y función de los tejidos nativos. Para lograr este objetivo, los científicos utilizan una variedad de técnicas como la impresión 3D, la microfabricación y el diseño de biomateriales.
Un aspecto crítico del éxito de la ingeniería de tejidos es garantizar que el órgano o tejido creado se integre perfectamente con los tejidos circundantes después de la implantación. Esto requiere una cuidadosa consideración de factores como la vascularización, la respuesta inmunológica y las propiedades biomecánicas.
A pesar de los significativos avances en la ingeniería de tejidos y la medicina regenerativa en las últimas décadas, todavía hay muchos desafíos que superar antes de que estos enfoques puedan ser ampliamente utilizados en entornos clínicos.
Uno de los principales obstáculos es lograr una funcionalidad y durabilidad a largo plazo de los tejidos creados. Otro desafío es desarrollar estrategias para prevenir el rechazo por parte del sistema inmunológico o minimizar las reacciones adversas a los materiales implantados.
Desafíos éticos y regulatorios
Los desafíos éticos y regulatorios asociados con la biotecnología son complejos y multifacéticos. Uno de los temas más controversiales es el uso de organismos modificados genéticamente (OMG) en la agricultura, lo que ha generado preocupaciones sobre posibles riesgos para la salud y el impacto ambiental.
La clonación humana es otro tema controvertido que plantea serias preguntas éticas sobre la creación de vida y nuestra responsabilidad hacia ella. Además, los derechos de propiedad intelectual plantean un desafío significativo para el desarrollo y la comercialización de innovaciones biotecnológicas, ya que pueden limitar el acceso al conocimiento científico y obstaculizar el progreso en este campo.
Organismos Genéticamente Modificados
Los Organismos Genéticamente Modificados (OGM) han sido ampliamente utilizados en el campo de la medicina por su capacidad para producir proteínas terapéuticas. Estos organismos son creados mediante la introducción de genes extranjeros en el genoma de un organismo, generalmente utilizando tecnología de ADN recombinante.
Los genes que se introducen codifican para proteínas específicas que pueden ser utilizadas para tratar enfermedades como la diabetes, la hemofilia y la fibrosis quística.
Al insertar estos genes en un organismo huésped, los científicos pueden crear un producto modificado genéticamente que produce grandes cantidades de la proteína deseada.
Si bien los OGM han sido beneficiosos en la producción de proteínas terapéuticas para uso médico, también existe controversia en torno a su uso. Una de las principales preocupaciones es el impacto ambiental potencial que los cultivos y la producción de alimentos GM pueden tener en los ecosistemas.
También existe preocupación en cuanto a la seguridad de consumir alimentos genéticamente modificados y si representan algún riesgo para la salud de humanos o animales.
A pesar de estas controversias, los OGM continúan desempeñando un papel importante en la medicina y la investigación, ya que ofrecen nuevas oportunidades para tratar enfermedades y mejorar la salud humana.
Clonación humana
La clonación humana es un tema controvertido en el campo de la medicina e investigación, ya que implica crear una copia genética idéntica de un ser humano. Los avances científicos han permitido la posibilidad de la clonación humana, pero las consideraciones éticas que rodean esta práctica son significativas.
Aquí hay tres puntos clave a considerar:
1) La clonación puede ser utilizada con fines reproductivos o terapéuticos. La clonación reproductiva implica crear un nuevo individuo con el mismo material genético que otra persona, mientras que la clonación terapéutica implica crear células madre que pueden ser utilizadas para tratar enfermedades o lesiones.
2) Mientras que algunos argumentan que la clonación reproductiva permitiría a parejas infértiles tener hijos, otros creen que plantea serias preocupaciones éticas sobre jugar a ser Dios y desvalorar la vida humana. Además, los individuos clonados pueden sufrir problemas de salud debido a las anormalidades causadas por el proceso de clonación.
3) La clonación terapéutica tiene beneficios potenciales para la investigación médica y el tratamiento de enfermedades como Parkinson y Alzheimer. Sin embargo, también hay preocupaciones acerca de utilizar embriones para experimentación y si esto constituye aprovecharse de poblaciones vulnerables.
A medida que los avances científicos continúan empujando los límites en el campo de la biotecnología, es importante que los investigadores y la sociedad en general consideren cuidadosamente tanto los beneficios potenciales como las implicaciones éticas de estas prácticas.

Futuro de la Biotecnología en Medicina.
El potencial de la biotecnología para revolucionar la medicina es evidente en el crecimiento proyectado del mercado global de biotecnología, que se espera que alcance los $526 mil millones para 2025. A medida que avanza la tecnología, surgen nuevos desafíos y oportunidades en el campo de la biotecnología.
Hay varios factores que darán forma al futuro de la biotecnología en la medicina, entre ellos los avances en la tecnología de edición de genes, la medicina personalizada y la inteligencia artificial.
Uno de los desafíos que enfrenta la biotecnología son las consideraciones éticas en torno a la tecnología de edición de genes. Si bien esta tecnología tiene el potencial de curar enfermedades genéticas, también plantea preguntas sobre la alteración de genes humanos con fines no médicos.
Otra oportunidad se encuentra en la medicina personalizada: tratamientos adaptados a la composición genética única de cada individuo. Este enfoque ha mostrado promesa en el tratamiento del cáncer y otras enfermedades con altas tasas de mutación.
La inteligencia artificial (IA) también presenta un futuro prometedor para la biotecnología en la medicina. Los algoritmos de aprendizaje automático pueden analizar grandes conjuntos de datos para identificar patrones y predecir resultados de manera más precisa que los humanos solos. Con la medicina de precisión cada vez más popular, la IA podría desempeñar un papel crucial en la identificación de planes de tratamiento óptimos basados en los datos de cada paciente.
El futuro de la biotecnología en la medicina tiene grandes promesas para mejorar la salud humana. Los avances en la tecnología de edición de genes, la medicina personalizada y la IA ofrecen oportunidades emocionantes para la innovación, pero también plantean consideraciones éticas que deben abordarse.
A medida que continuamos explorando estas tecnologías emergentes, es importante equilibrar la innovación con el uso responsable y la consideración de su impacto en la sociedad en su conjunto.
| Desafíos | Oportunidades |
|---|---|
| Consideraciones éticas en torno a la edición de genes | Medicina personalizada |
| Equilibrar la innovación con el uso responsable | Avances en la tecnología de edición de genes |
| Impacto en la sociedad en su conjunto | Inteligencia artificial |
Preguntas frecuentes
¿Cuáles son algunos ejemplos específicos de medicamentos biológicos producidos a través de la biotecnología?
La biotecnología ha revolucionado el desarrollo de medicamentos y ha llevado a la producción de una variedad de medicamentos biológicos.
Estos incluyen anticuerpos monoclonales, proteínas recombinantes y vacunas.
Los anticuerpos monoclonales se utilizan para tratar el cáncer, enfermedades autoinmunitarias y enfermedades infecciosas al dirigirse a células o proteínas específicas en el cuerpo.
Por ejemplo, el trastuzumab es un anticuerpo monoclonal que se dirige a las células de cáncer de mama HER2 positivas.
Las proteínas recombinantes, como la insulina, se producen utilizando técnicas de biotecnología para el tratamiento de la diabetes.
Las vacunas también se desarrollan utilizando biotecnología para estimular una respuesta inmunitaria contra agentes infecciosos como virus y bacterias.
Ejemplos incluyen la vacuna del virus del papiloma humano (VPH) y la vacuna contra la gripe.
La biotecnología ha permitido un mayor enfoque preciso de las enfermedades a nivel molecular, lo que lleva a tratamientos más efectivos con menos efectos secundarios que los medicamentos tradicionales.
¿En qué se diferencia la ingeniería de tejidos de los métodos de trasplante tradicionales?
La ingeniería de tejidos es una técnica novedosa utilizada en medicina regenerativa que difiere de los métodos tradicionales de trasplante. El trasplante tradicional implica la transferencia de órganos enteros o parciales de un donante a un receptor, mientras que la ingeniería de tejidos se centra en la creación de tejidos y órganos funcionales combinando células, biomateriales y factores de crecimiento.
Los enfoques de la ingeniería de tejidos se pueden dividir en dos categorías: organogénesis y terapias celulares. La organogénesis implica el uso de materiales de andamiaje para crear estructuras tridimensionales que se asemejan a órganos naturales, que luego se siembran con células y se cultivan en condiciones específicas para promover el desarrollo del órgano.
Las terapias celulares implican la entrega de tipos celulares específicos a tejidos u órganos dañados para mejorar su función o promover la regeneración.
Si bien ambos enfoques han demostrado ser prometedores en estudios preclínicos y ensayos clínicos, todavía hay numerosos desafíos antes de que puedan utilizarse rutinariamente en el cuidado de pacientes, incluida la escalabilidad, la aprobación regulatoria y las preocupaciones de seguridad a largo plazo.
A pesar de estos desafíos, la ingeniería de tejidos representa una emocionante vía para desarrollar nuevos tratamientos para enfermedades y lesiones crónicas.
¿Cuáles son algunas preocupaciones éticas comunes en torno al uso de la biotecnología en la medicina?
El uso de la biotecnología en medicina ha llevado a importantes avances en el tratamiento de enfermedades y en la salvación de vidas a nivel molecular. Sin embargo, las implicaciones éticas del uso de la biotecnología han sido un tema de discusión entre expertos y el público en general.
Una preocupación común se relaciona con la ingeniería genética, que plantea preguntas sobre la alteración del ADN humano y la creación de "bebés diseñados". Otras preocupaciones incluyen el uso de pruebas en animales, el acceso a tratamientos costosos solo para aquellos que pueden pagarlos y las preocupaciones de privacidad con respecto a los datos genéticos.
La percepción pública también juega un papel crucial en la formación de consideraciones éticas en torno a la biotecnología. A pesar de sus posibles beneficios, es esencial abordar estas preocupaciones éticas de manera proactiva y transparente asegurando que cualquier avance realizado a través de la biotecnología beneficie a la sociedad en su conjunto.
¿Existen marcos regulatorios actuales para el uso de la biotecnología en la medicina?
Se han establecido directrices regulatorias para garantizar el uso seguro y ético de la biotecnología en la medicina. En los Estados Unidos, la Administración de Alimentos y Medicamentos (FDA) tiene autoridad sobre la regulación de productos de biotecnología utilizados en tratamientos médicos.
La FDA evalúa estos productos en cuanto a seguridad, eficacia y calidad antes de otorgar la aprobación para su uso. Además, existen implicaciones legales asociadas con el uso de la biotecnología en la medicina que deben considerarse.
Por ejemplo, las leyes de patentes pueden afectar el desarrollo y la disponibilidad de ciertos tratamientos o tecnologías.
En general, es crucial que existan marcos regulatorios para promover el uso responsable de la biotecnología en la medicina, al mismo tiempo que se protege la salud pública y se garantiza el acceso a tratamientos que salvan vidas.
¿Qué nuevos avances o desarrollos podemos esperar en el futuro de la biotecnología en la medicina?
El futuro de la biotecnología en la medicina es prometedor, con numerosas aplicaciones e innovaciones potenciales en el horizonte.
Un avance que tiene gran promesa es la tecnología de edición genética, que tiene el potencial de curar enfermedades genéticas corrigiendo genes defectuosos a nivel molecular.
Otra área de avance potencial es la medicina personalizada, donde los tratamientos se adaptan a la composición genética única de cada individuo.
Además, los avances en biología sintética podrían llevar al desarrollo de medicamentos y terapias completamente nuevos.
Estas futuras innovaciones tienen el potencial de revolucionar la medicina ofreciendo tratamientos más precisos y efectivos para una amplia gama de enfermedades.
A medida que la investigación continúa en estas áreas, podemos esperar aún más avances que mejorarán aún más la salud humana y salvarán innumerables vidas.
Conclusión
La biotecnología ha revolucionado la forma en que abordamos la medicina, permitiéndonos desarrollar tratamientos nuevos y más efectivos para una amplia gama de enfermedades. Al aprovechar el poder de los organismos vivos, la biotecnología nos permite producir medicamentos biológicos con mayor precisión y eficacia que nunca.
Además, ha abierto nuevas fronteras en técnicas de diagnóstico, ingeniería de tejidos y medicina regenerativa.
Un área clave donde la biotecnología es particularmente útil es en la producción de anticuerpos monoclonales, que se utilizan para tratar una variedad de afecciones, incluyendo cáncer, trastornos autoinmunitarios y enfermedades infecciosas.
Estas moléculas complejas son producidas por células genéticamente modificadas que han sido programadas para producir proteínas específicas. Esto permite a los investigadores crear terapias altamente dirigidas que pueden atacar selectivamente las células enfermas sin dañar las sanas.
Sin embargo, como con cualquier nueva tecnología, también hay desafíos éticos y regulatorios asociados con la biotecnología en medicina.
Por ejemplo, se han planteado preocupaciones sobre la seguridad de los organismos modificados genéticamente (OMG) utilizados en algunos procesos biotecnológicos. También hay preguntas sobre quién debería tener acceso a estos tratamientos de vanguardia y cómo deberían ser regulados.
A pesar de estos desafíos, el futuro se ve brillante para la biotecnología en medicina. Con investigación continua sobre nuevas aplicaciones para este emocionante campo de la ciencia y la inversión continua tanto del sector público como del privado, podemos esperar muchos más avances en los años venideros. Como dice una famosa figura retórica: 'El cielo es el límite'. De hecho, cuando se trata de biotecnología en medicina, parece que no hay fin a lo que podemos lograr.
Si quieres conocer otros artículos parecidos a ¿Dónde se utiliza la biotecnología en la medicina? - Salvando vidas a nivel molecular. puedes visitar la categoría Biotecnología.
Deja una respuesta




¡Más Contenido!